2025年7月30日,一篇题为" TUBB3/DTX LNPs Dry Powder Inhaler and an Efficient Delivery Device for Targeted Therapy of Lung Cancer "的研究论文,发表在《ACS Applied Materials & Interfaces》杂志上。

为解决siRNA-LNP载体的制备与纯化难题,本研究借助艾特森MPE-L2型微流控制备仪与LDS-L2型超滤设备开展相关实验。其中,艾特森微流控设备可实现脂质纳米粒的精准制备,保障载体粒径均一性与包封率;超滤设备则能高效完成载体的分离纯化,去除游离药物与杂质,提升siRNA-LNP的纯度与稳定性,为后续构建兼具肺靶向、缓释性和稳定性的协同治疗平台奠定设备基础。


研究背景
肺癌是全球 “癌王” 级恶性肿瘤,高耐药性、强全身毒性和差预后一直是治疗难题。作为肺癌一线化疗药,多西他赛(DTX)水溶性极差,还容易让肿瘤产生耐药性,这与βIII - 微管蛋白(TUBB3)过表达直接相关。TUBB3-siRNA能通过RNA干扰下调TUBB3,本是逆转耐药的理想手段,却面临体内外核酸酶降解、难以跨细胞膜的困境。
脂质纳米粒(LNPs)可同时包裹多西他赛和TUBB3-siRNA,是具潜力的递送载体,但其胶体溶液需低温储运,存在运输不便、成本高昂的问题。此外,传统干粉吸入装置无法适配吸湿性强、稳定性差的siRNA-LNP粉末,缺乏高效的单剂量递送方案。因此,打造一个兼具肺靶向、缓释性和稳定性的协同治疗平台,搭配专用递送装置,成为突破肺癌治疗瓶颈的关键。
1. TUBB3/多西他赛-脂质纳米粒可吸入干粉制备流程图
首先,图1展示了TUBB3/多西他赛-脂质纳米粒从液体胶体经喷雾冷冻干燥技术制备为可吸入干粉的流程,明确了研究的核心制剂转化路径,为后续性能验证奠定基础。

图例1:TUBB3/多西他赛-脂质纳米粒可吸入干粉制备流程图
➤ TUBB3/多西他赛-脂质纳米粒配方:

图例2:TUBB3/多西他赛-脂质纳米粒配方
2. 脂质纳米粒及干粉的粒径与ζ电位特征
其次,图3呈现了刚制备LNPs溶液与喷雾冷冻干燥后脂质纳米粒的粒径分布及ζ电位特征,显示两类脂质纳米粒粒径均小于200nm、ζ电位接近0mV,干粉D50在1.99-5.90μm之间,证明喷雾冷冻干燥工艺未显著改变脂质纳米粒核心理化性质,且干粉粒径符合肺部沉积要求。
 图例3:脂质纳米粒及干粉的粒径与ζ电位特征
图例3:脂质纳米粒及干粉的粒径与ζ电位特征
3. 脂质纳米粒及干粉的形态表征
接着,图4通过透射电子显微镜和扫描电子显微镜图像,展示了新鲜脂质纳米粒、复水后喷雾冷冻干燥脂质纳米粒及干粉的形态,新鲜和复水脂质纳米粒均为均匀球形,干粉呈疏松多孔球形,证实喷雾冷冻干燥过程保留了脂质纳米粒结构完整性,且干粉形态利于分散和肺部递送。
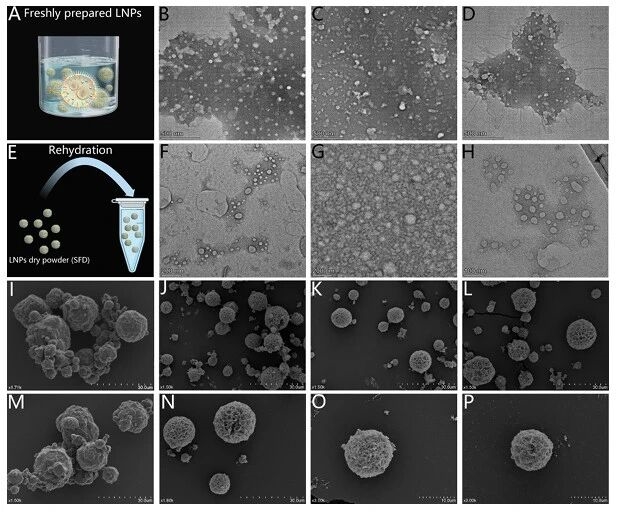
图例4:脂质纳米粒及干粉的形态表征
4. 脂质纳米粒细胞摄取及siRNA完整性验证
研究团队通过图5结果,证明TUBB3-siRNA被A549细胞成功摄取且与脂质纳米粒外壳共定位,喷雾冷冻干燥前后siRNA结构完整,证明脂质纳米粒可有效递送siRNA,且喷雾冷冻干燥工艺不破坏siRNA完整性。
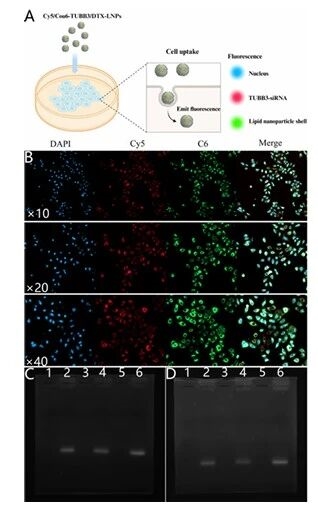
图例5:脂质纳米粒细胞摄取及siRNA完整性验证
5.脂质纳米粒的细胞毒性、凋亡诱导及协同机制
随后,图6证明了TUBB3/多西他赛-脂质纳米粒对BEAS-2B细胞生物相容性好,对H460和A549细胞抑制作用显著,凋亡率高于单药组,TUBB3-siRNA可下调TUBB3表达、抑制p-AKT通路,揭示化疗与基因治疗的协同抗肿瘤机制,且喷雾冷冻干燥工艺不影响制剂生物活性。
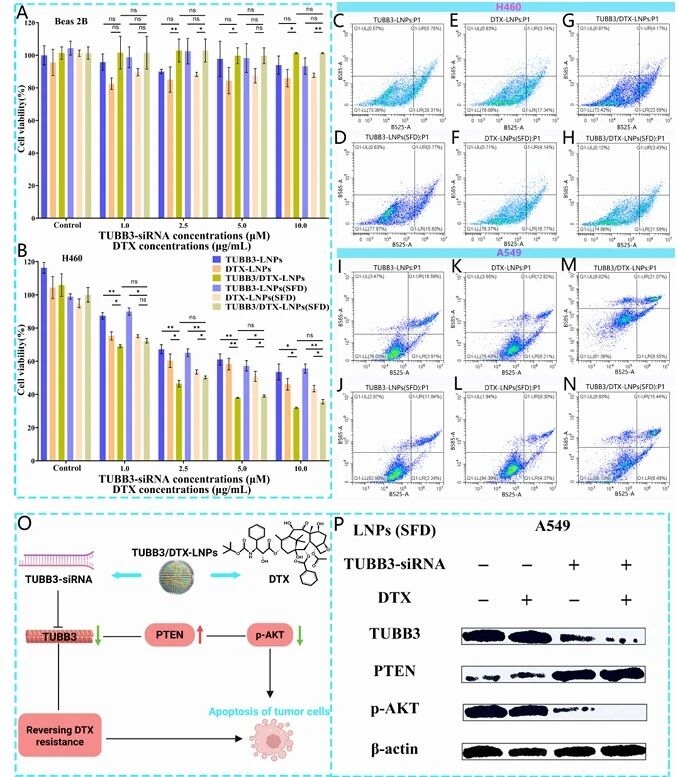
图例6:脂质纳米粒的细胞毒性、凋亡诱导及协同机制
6. 单剂量干粉吸入装置结构与排空率
图7展示了单剂量干粉吸入装置的结构示意图、实物图及不同装置的干粉排空率数据,装置采用中部对称四通风口设计,排空率达95%-100%,说明该装置结构合理,能实现高效干粉递送。

图例7:单剂量干粉吸入装置结构与排空率
7. 干粉吸入装置吸入原理及体外气溶胶沉积
图8呈现了干粉吸入装置的吸入示意图及体外气溶胶在下一代撞击器中的沉积模式,显示制剂输出效率>90%,质量中值空气动力学直径约2.61μm,证明制剂与装置适配性良好,具备理想的肺部递送空气动力学特性。

图例8:干粉吸入装置吸入原理及体外气溶胶沉积
8. 脂质纳米粒干粉的肺靶向性与生物安全性
图9实验结果显示由Cy5.5标记的脂质纳米粒干粉主要富集于肺部且48小时内持续滞留,主要器官无明显病理损伤,证实制剂具有强肺靶向性和良好生物安全性。
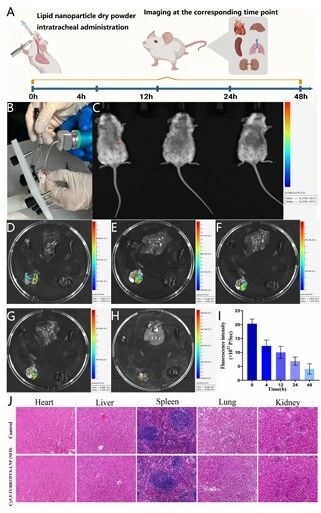
图例9:脂质纳米粒干粉的肺靶向性与生物安全性
9. 不同给药方式的药代动力学与组织分布
最后,图10展示了气管内给药与静脉给药后血清及肺组织中多西他赛浓度变化、不同时间点组织分布数据,显示气管内给药组肺组织药物浓度显著高于静脉给药组,血清药物浓度平稳且持续时间长,证明气管内给药结合制剂与装置可实现肺部靶向富集和长效缓释,降低全身暴露。
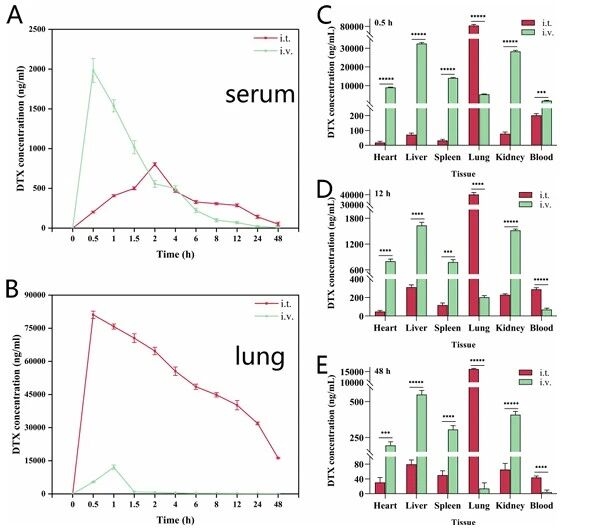
图例10:不同给药方式的药代动力学与组织分布
知识分享:研究亮点
1 创新构建化疗与基因治疗协同体系,通过微流控技术将多西他赛与TUBB3-siRNA共包封制备脂质纳米粒,协同逆转耐药、增强抗肿瘤效果。
2 采用喷雾冷冻干燥技术制备可吸入干粉,解决核酸药物水性制剂稳定性差、需低温储运的难题,同时获得适宜肺部沉积的空气动力学特性。
3 研发对称四通风口单剂量预填充吸入装置,实现近完全干粉排空,结合气管内给药达成肺部靶向富集与长效缓释,显著降低全身毒性。
参考文献:
ACS Applied Materials & Interfaces ( IF 8.2 ) Pub Date : 2025-07-30 , DOI: 10.1021/acsami.5c07808.
 欢迎来到苏州艾特森制药设备有限公司网站!
欢迎来到苏州艾特森制药设备有限公司网站! 欢迎来到苏州艾特森制药设备有限公司网站!
欢迎来到苏州艾特森制药设备有限公司网站!




 图例3:脂质纳米粒及干粉的粒径与ζ电位特征
图例3:脂质纳米粒及干粉的粒径与ζ电位特征





