2025年11月07日 中国科学院武汉病毒研究所等单位在《Vaccine》上发表题为" Modular design of a self-amplifying mRNA vaccine for multivalent immunization against Neisseria meningitidis B"的研究论文。

研究团队通过艾特森MPE-L2型微流控制备仪制备mRNA-LNP疫苗,成功开发出一款 “效价高、工艺优、成本低” 的MenB多价SAM疫苗,并建立了一套可复制的多价细菌mRNA疫苗开发平台。

研究背景
B型脑膜炎奈瑟菌(MenB)是引发细菌性脑膜炎和败血症的主要病原体之一,对婴幼儿、青少年及免疫功能低下的人群危害显著;其疫苗研发长期受限于荚膜多糖免疫原性弱且与人神经细胞黏附分子结构相似、外膜蛋白抗原变异性大及免疫逃逸机制复杂等问题,现有的临床蛋白疫苗存在生产工艺复杂、成本高、免疫持久性不足等缺陷。
自扩增mRNA(SAM)技术平台凭借抗原设计灵活、生产简便、免疫原性强且具剂量节约潜力的优势,为突破上述困境提供了新可能,但多价细菌mRNA疫苗开发仍面临抗原竞争、表达不均等挑战,亟需优化抗原设计与制剂工艺以实现多抗原均衡呈递与功能协同。
1. 疫苗设计

2. mRNA-LNP疫苗制备

图例1:LNP筛选过程
3. 串联抗原mRNA构建体设计与表征
研究团队首先通过串联抗原mRNA构建体的设计与基础表征,明确串联抗原NRM与SAM平台的结构差异,同时借助琼脂糖凝胶电泳验证12种串联抗原mRNA的分子大小与理论预期一致,为后续免疫实验构建核心研究材料。
串联抗原设计:将四种抗原通过柔性链接肽融合为单一蛋白,并编码于自复制mRNA(SAM)或非复制mRNA(NRM)中,同时分别在蛋白N端整合6种信号肽进行筛选。
单抗原混合设计:分别编码单个抗原的SAM,通过预混合(PreMix)或后混合(PostMix)方式封装于脂质纳米颗粒(LNP)中。

图例2:抗原mRNA构建体设计与表征
4. SAM与NRM平台体液免疫原性对比
在此基础上,研究团队通过开展SAM与NRM平台的体液免疫原性对比,结合标准化小鼠免疫程序,检测不同时间点血清中四种抗原的特异性IgG抗体滴度,明确SAM平台在激发体液免疫方面具有显著优势。
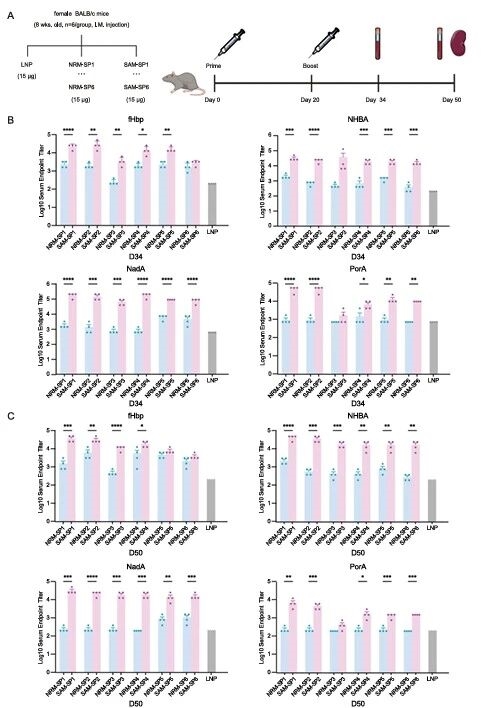
图例3:SAM与NRM平台体液免疫原性对比
5.疫苗诱导的T细胞活化及IFN-γ分泌
随后,研究团队从细胞免疫层面进一步验证该结论,通过流式细胞术分析T细胞活化标志物的表达,结合ELISpot试验定量抗原特异性IFN-γ的分泌水平,全面证实SAM平台在诱导功能性细胞免疫应答中的核心价值优势。

图例4:疫苗诱导的T细胞活化及IFN-γ分泌
6. 单抗原混合与串联构建体免疫原性比较
为解决串联构建体体外表达不足的问题,研究团队通过提出单抗原混合策略,系统比较单抗原PreMix/PostMix策略与串联构建体(SAM-SP2)的体液免疫效果,验证单抗原混合策略的可行性与优越性。

图例5:单抗原混合与串联构建体免疫原性比较
7. 不同剂量疫苗的体液免疫应答
基于上述优化策略,研究团队进一步开展剂量梯度研究,设置1μg、5μg、15μg三个剂量组,分析不同剂量下三种疫苗策略的多抗原特异性抗体应答,为临床剂量选择提供关键数据支撑。

图例6:不同剂量疫苗的体液免疫应答
8. 不同剂量疫苗的细胞免疫应答特征
最后,研究团队聚焦不同剂量疫苗的细胞免疫应答特征,通过流式细胞术和ELISpot试验,明确PreMix/PostMix组在各剂量下均能有效激活T细胞活化与IFN-γ分泌,结合后续血清杀菌试验结果,最终确立SAM-PreMix策略的综合优势,为多价细菌mRNA 疫苗研发提供完整解决方案。

图例7:不同剂量疫苗的细胞免疫应答特征
知识分享:研究亮点
1 创新构建 “单抗原平行表达+自扩增mRNA(SAM)” 多价疫苗框架,通过串联融合与PreMix/PostMix两种混合制剂策略的系统对比,解决了传统多抗原疫苗抗原竞争、表达不均的核心问题。
2 首次证实SAM平台相比非复制型mRNA(NRM),在低剂量下即可诱导更强的体液免疫与细胞免疫应答,且具备显著剂量节约潜力,突破了传统蛋白疫苗免疫持久性不足的局限。
3 明确 SAM-PreMix策略在免疫原性(血清杀菌滴度达 1:256)、功能保护及生产工艺标准化、可扩展性上的综合优势,为复杂细菌病原体多价 mRNA 疫苗研发提供了模块化、通用型技术方案。
参考文献:
Vaccine Pub Date : 2025-11-07 , DOI: 10.1016/j.vaccine.2025.127964.
 欢迎来到苏州艾特森制药设备有限公司网站!
欢迎来到苏州艾特森制药设备有限公司网站! 欢迎来到苏州艾特森制药设备有限公司网站!
欢迎来到苏州艾特森制药设备有限公司网站!








